
基本情報
|
2025年11月28日 |
|
| インチュニブ錠「使用上の注意」改訂のお知らせ | |
|
2025年02月03日 |
|
| インチュニブ錠1mg、3mgは徐放性製剤です~分割、粉砕、かみ砕いての処方・投与・服用はしないでください~ | |
|
2024年07月23日 |
|
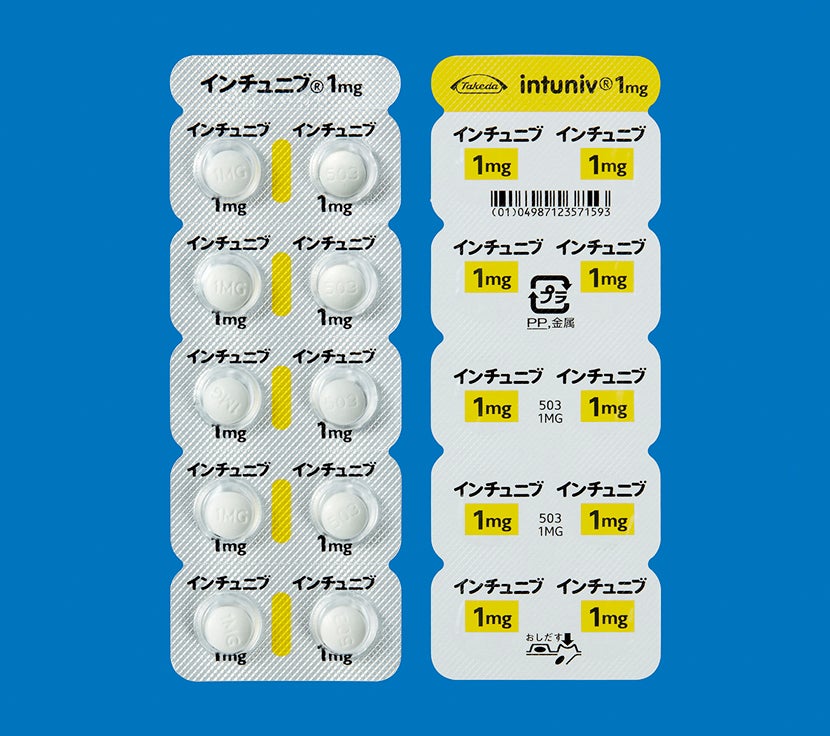
| インチュニブ錠1mg・3mgのPTPシート、アルミピロー及び組箱変更のご案内(2024年7月) |
製品・疾患紹介動画
製品に関するWeb講演会
製品に関するWeb講演会
動物実験(マウス)において大量投与により催奇形作用(外脳症、脊椎破裂症)が報告されていることから、妊婦又は妊娠している可能性のある女性への投与は禁忌です。
妊娠可能な女児・女性については、適切に避妊等を行うよう指導してください。
(参考資料)
1) インチュニブ錠1㎎・3㎎ 電子添文
2) インチュニブ錠1㎎・3㎎ 適正使用ガイド
動物実験(ラット)で乳汁中への移行が認められていることから、インチュニブ錠投与中は治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続または中止を検討してください。
なお、ヒトでの検討データはなく、ヒトの乳汁中への移行については不明です。
また、2025年12月現在、インチュニブ投与中止後の授乳再開時期について、参考となる情報は入手していません。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
・インチュニブ錠1㎎・3㎎ インタビューフォーム
【インチュニブ錠を休薬する場合】
休薬期間を設けるにあたり、インチュニブ錠の投与を急に中止して休薬すると、反跳現象として血圧及び脈拍数が一過性に上昇する可能性があります。インチュニブ錠を休薬する際は、その影響を最小限に抑えるためにも、原則として3日間以上の間隔をあけて1mgずつ、血圧及び脈拍数を測定するなど患者の状態を十分に観察しながら徐々に減量して休薬してください。
【インチュニブ錠の服薬を再開する場合】
休薬後の再開の際は、休薬前の投与量で急に再開すると血圧低下及びそれに付随する副作用が発現する可能性がありますので、初回投与時と同様、低用量から開始し、段階的に増量してください。 また、血圧・脈拍を定期的に確認し、副作用(過度の血圧低下、徐脈など)に留意してください。
(参考資料)
・インチュニブ錠1㎎・3㎎ 適正使用ガイド
・インチュニブ錠1㎎・3㎎ 電子添文
健康成人 140 例を対象に、3mg(1mg 錠 3 錠あるいは 3mg 錠 1錠)単回投与時の食事の影響を検討したところ、空腹時投与に比べて食後投与(高脂肪食) では Cmax は約 1.2~1.4 倍高く、AUC は約 1.2~1.3 倍高いという結果でした。
ただし通常食摂取による薬物動態への影響は大きなものではないと考えられ、用法用量として食事に関する注意や制限はありません。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
・インチュニブ錠1㎎・3㎎ 申請資料概要(2017/3/30承認)、2.7.1.3.2 食事の影響、p.14-15
https://www.pmda.go.jp/drugs/2017/P20170412001/340018000_22900AMX00511000_K100_1.pdf#page=1
半錠で(分割して)の投与は承認外です。またインチュニブは徐放性製剤のため半錠での投与はできません。
インチュニブの電子添文「適用上の注意」薬剤交付時の注意に、本剤は徐放性製剤であるため、割ったり、砕いたり、すりつぶしたりしないで、そのままかまずに服用するよう指導すること、と記載されています。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
インチュニブ錠は徐放性製剤のため、粉砕はできません。
インチュニブの電子添文「適用上の注意」薬剤交付時の注意に、本剤は徐放性製剤であるため、割ったり、砕いたり、すりつぶしたりしないで、そのままかまずに服用するよう指導すること、と記載されています。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
国内の添付文書において、飲み忘れた際の対処法は定められておりません。
(参考)
【米国】2回以上連続して飲み忘れた後に、患者がそれまでの維持用量を再開する場合は、患者の忍容性に応じて漸増を検討する。
【欧州】飲み忘れがあった場合、本剤の投与を翌日に再開してもよい。2回以上連続して飲み忘れがあった場合は、患者の本剤に対する忍容性に応じて際漸増が推奨される。
(参考資料)
・インチュニブ錠1㎎・3㎎ 適正使用ガイド
・インチュニブ錠1㎎・3㎎ インタビューフォーム
分包後(単剤での分包、他剤との一包化)の安定性は検討していません。
ご参考までに PTPから出した場合の安定性をご紹介します。
曝光・温度25℃・湿度60%RHという条件の下実施した製剤の安定性試験(苛酷試験)において、インチュニブ1mg錠、3mg錠ともに変化は認められませんでした。
保存期間 120万lx・hr*
*4000lxの照射で、120万lx・hrとなるには300時間かかります。
(参考資料)
・インチュニブ錠1㎎・3㎎ インタビューフォーム
インチュニブ錠は「流通・処方管理プログラム対象薬剤」ではないため、医師や薬剤師の、eラーニング受講や登録制度による処方管理はありません。
通常の医療用医薬品と同じ取り扱いをお願いいたします。
簡易懸濁法を含む経管投与は承認外用法です。また、インチュニブ錠は徐放性製剤であることから、経管投与(簡易懸濁法)はできません。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
インチュニブは主にCYP3A4/5で代謝される薬剤(基質)であり、クラリスロマイシンは、CYP3A4/5阻害剤であることから、インチュニブの血中濃度が上昇し、作用が増強するおそれがあるため、併用注意としています。
併用する場合には、年齢や体重に関わらず、インチュニブの投与は1日1mgより開始し、定期的に血圧及び脈拍数を測定するなど、患者の状態を注意深く観察してください。また、患者(小児の場合には、患者及び保護者又はそれに代わる適切な者)に対しては、なんらかの異常が認められた場合は速やかに医療機関に連絡するようご指導ください。特に、50kg未満の小児については、投与開始時の血中濃度としては、国内の承認時までの臨床試験において経験のない濃度に上昇する可能性があります。そのため、これらの患者に本剤を投与する場合は、より注意してください。
なお、臨床試験においてクラリスロマイシンとの薬物相互作用試験は実施されておらず、併用した場合の薬物動態に関するデータはありません。
(参考資料)
・インチュニブ錠1㎎・3㎎ 電子添文
・インチュニブ錠1㎎・3㎎ 適正使用ガイド
各ボタンはくすりの適正使用協議会サイトにリンクします。
- 「くすりのしおり」は、くすりの適正使用協議会が定めた基本フォーマットにしたがって作成しております。 詳しくは、「くすりのしおり」トップページをご参照ください。
- 「くすりのしおり」は作成時点の電子添文に基づいておりますが、電子添文に記載された全ての情報を網羅してはおりません。服薬指導資料を作成される際には、最新の電子添文などをご確認いただき、その患者さんにとって必要な注意事項や、医療機関の実情に合わせて加筆修正のうえ、ご利用くださいますようにお願い申し上げます。
- 「くすりのしおり」のご利用によって、直接または間接的に損害が生じても、弊社はいかなる責任も負いません。
















![インチュニブ®を飲んでいるみなさまへ[服薬指導箋]](https://www.takedamed.com/sites/default/files/2023-09/INT_%E3%82%A4%E3%83%B3%E3%83%81%E3%83%A5%E3%83%8B%E3%83%96%C2%AE%E3%82%92%E9%A3%B2%E3%82%93%E3%81%A7%E3%81%84%E3%82%8B%E3%81%BF%E3%81%AA%E3%81%95%E3%81%BE%E3%81%B8%5B%E6%9C%8D%E8%96%AC%E6%8C%87%E5%B0%8E%E7%AE%8B%5D%28%E5%B0%8F%E5%85%90%E7%94%A8%29.png)
![インチュニブ®を飲んでいるみなさまへ[患者冊子]](https://www.takedamed.com/sites/default/files/2023-11/%E3%82%B9%E3%82%AF%E3%83%AA%E3%83%BC%E3%83%B3%E3%82%B7%E3%83%A7%E3%83%83%E3%83%88%202023-11-17%20115617.png)



![インチュニブ®を飲んでいるみなさまへ[服薬指導箋]](https://www.takedamed.com/sites/default/files/2024-08/%E3%80%90%E8%A1%A8%E7%B4%99%E3%80%912-5-7647_%E3%82%A4%E3%83%B3%E3%83%81%E3%83%A5%E3%83%8B%E3%83%96%E3%82%92%E9%A3%B2%E3%82%93%E3%81%A7%E3%81%84%E3%82%8B%E3%81%BF%E3%81%AA%E3%81%95%E3%81%BE%E3%81%B8%EF%BC%88%E6%88%90%E4%BA%BA%EF%BC%89%E3%80%90%E6%8C%87%E5%B0%8E%E7%AE%8B%E3%80%91_0.png)
![インチュニブ®を飲んでいるみなさまへ[患者冊子]](https://www.takedamed.com/sites/default/files/2023-09/INT_%E3%82%A4%E3%83%B3%E3%83%81%E3%83%A5%E3%83%8B%E3%83%96%C2%AE%E3%82%92%E9%A3%B2%E3%82%93%E3%81%A7%E3%81%84%E3%82%8B%E3%81%BF%E3%81%AA%E3%81%95%E3%81%BE%E3%81%B8%5B%E6%82%A3%E8%80%85%E5%86%8A%E5%AD%90%5D.png)




