CIDPの治療
<p>CIDP(慢性炎症性脱髄性多発根ニューロパチー)</p>
監修:竹下 幸男 先生(山口大学医学部 神経・筋難病治療学講座/血液脳神経関門先進病態創薬研究講座 教授)
CIDPの治療⽬的
CIDPは脱髄疾患であり、免疫療法によって脱髄を阻⽌し、髄鞘の再⽣を促すことで回復が期待できる疾患です。髄鞘への免疫反応が強い症例、⻑期間未治療の症例、⼜は不⼗分な治療が継続された症例では、⼆次的軸索変性が⽣じ、治療反応性が低下したり後遺症を残す可能性が⾼くなります1)。
CIDPの治療⽬的は、①現在の症状を改善させること(導⼊療法)、②病勢を沈静化させ再燃を防ぐこと(維持療法)です2)。
図1. CIDPの病態(イメージ図)
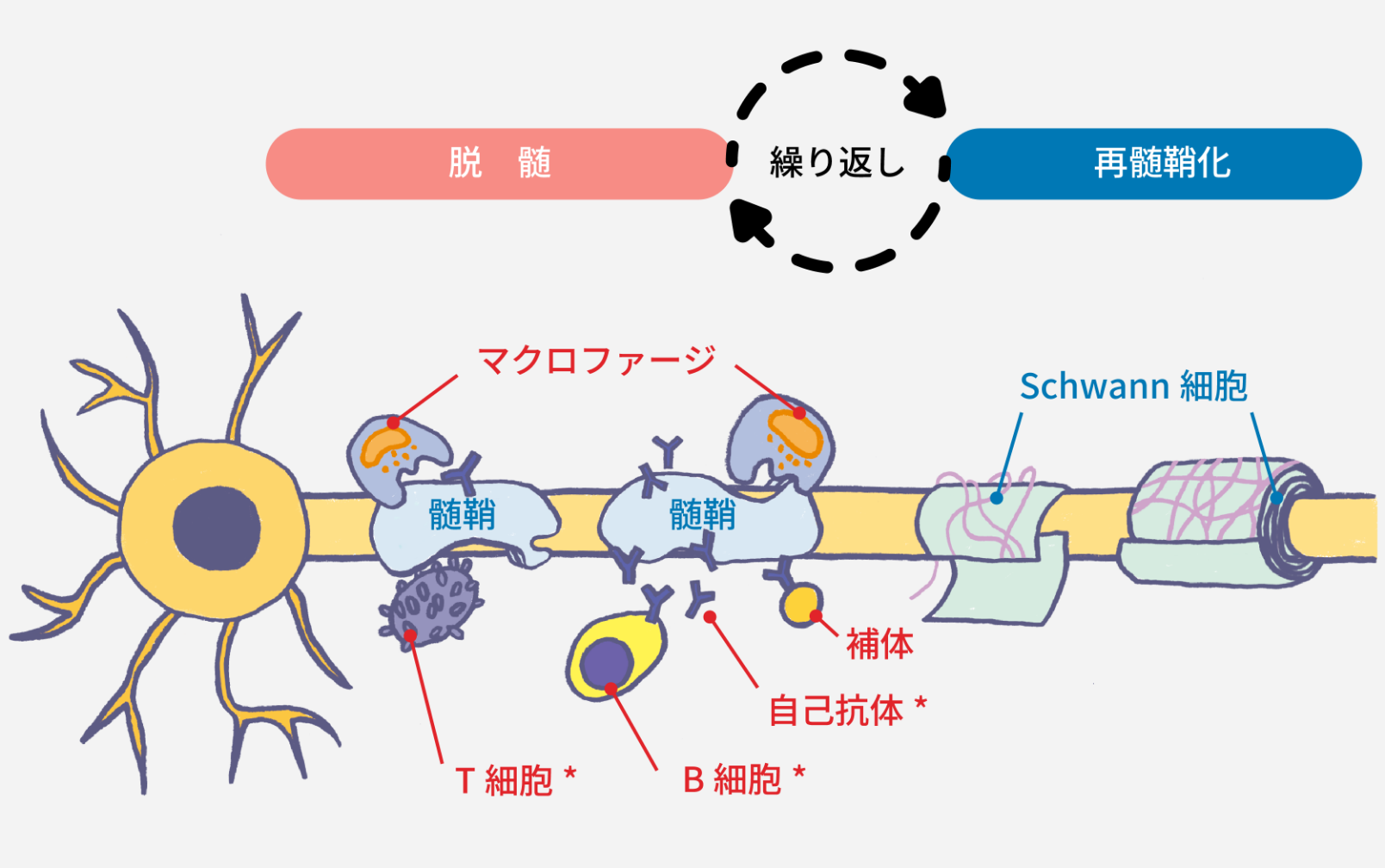
*液性免疫(B細胞系、抗体)と細胞性免疫(T細胞系)の両者が関与すると考えられます。
⽇本神経学会(監): 慢性炎症性脱髄性多発根ニューロパチー, 多巣性運動ニューロパチー診療ガイドライン 2024,南江堂. 2024: 2-6.より作図
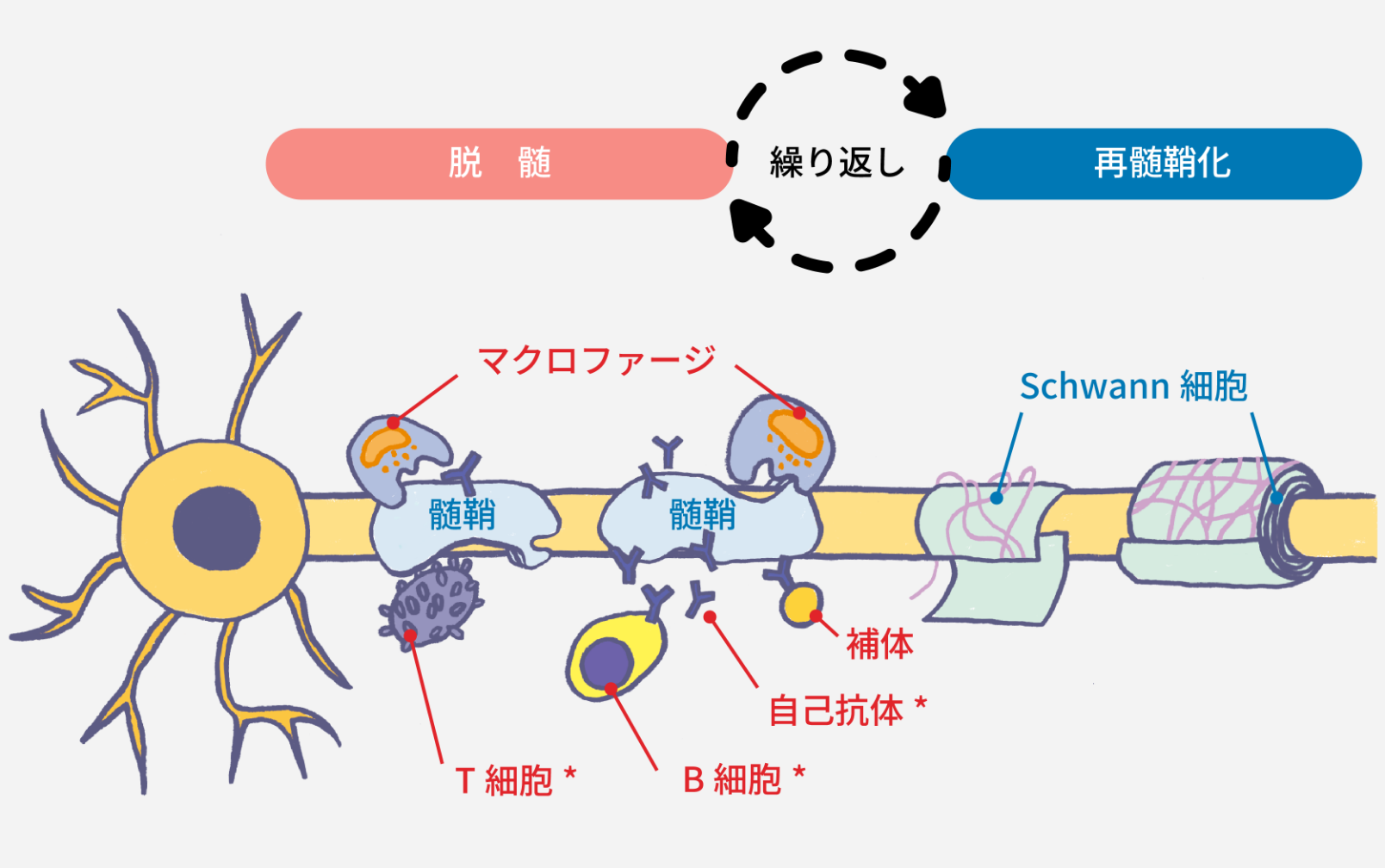
*液性免疫(B細胞系、抗体)と細胞性免疫(T細胞系)の両者が関与すると考えられます。
⽇本神経学会(監): 慢性炎症性脱髄性多発根ニューロパチー, 多巣性運動ニューロパチー診療ガイドライン 2024,南江堂. 2024: 2-6.より作図
CIDPの治療
CIDPの治療は、発症時の疾患活動期における寛解導⼊のための治療(導⼊療法)と、寛解状態を維持するための治療(維持療法)の2つに⼤別されます。導⼊療法の第⼀選択は免疫グロブリンと副腎⽪質ステロイド薬であり、両者とも⼗分な効果が得られない場合は⾎漿交換療法を⾏います3)。維持療法は、免疫グロブリン静注療法(IVIg)と免疫グロブリン⽪下注療法(SCIg)ともに推奨されています。副腎⽪質ステロイド薬も導⼊療法から減量し、⻑期的効果が期待できます。いずれも導⼊療法に⽤いられた治療を維持療法として使⽤されます3)。
これらの治療法は、複数のランダム化⽐較試験により⾼いエビデンスレベルが⽰されています。ただし、これらの研究結果は主にCIDP全体の60〜70%を占める典型的CIDPに基づくものであり、病型別のエビデンスは存在しません。遠位型CIDPや多巣型CIDPなどのバリアントに対する治療は、まだ確⽴されていません3)。
図2. 3つの主な治療の位置づけ
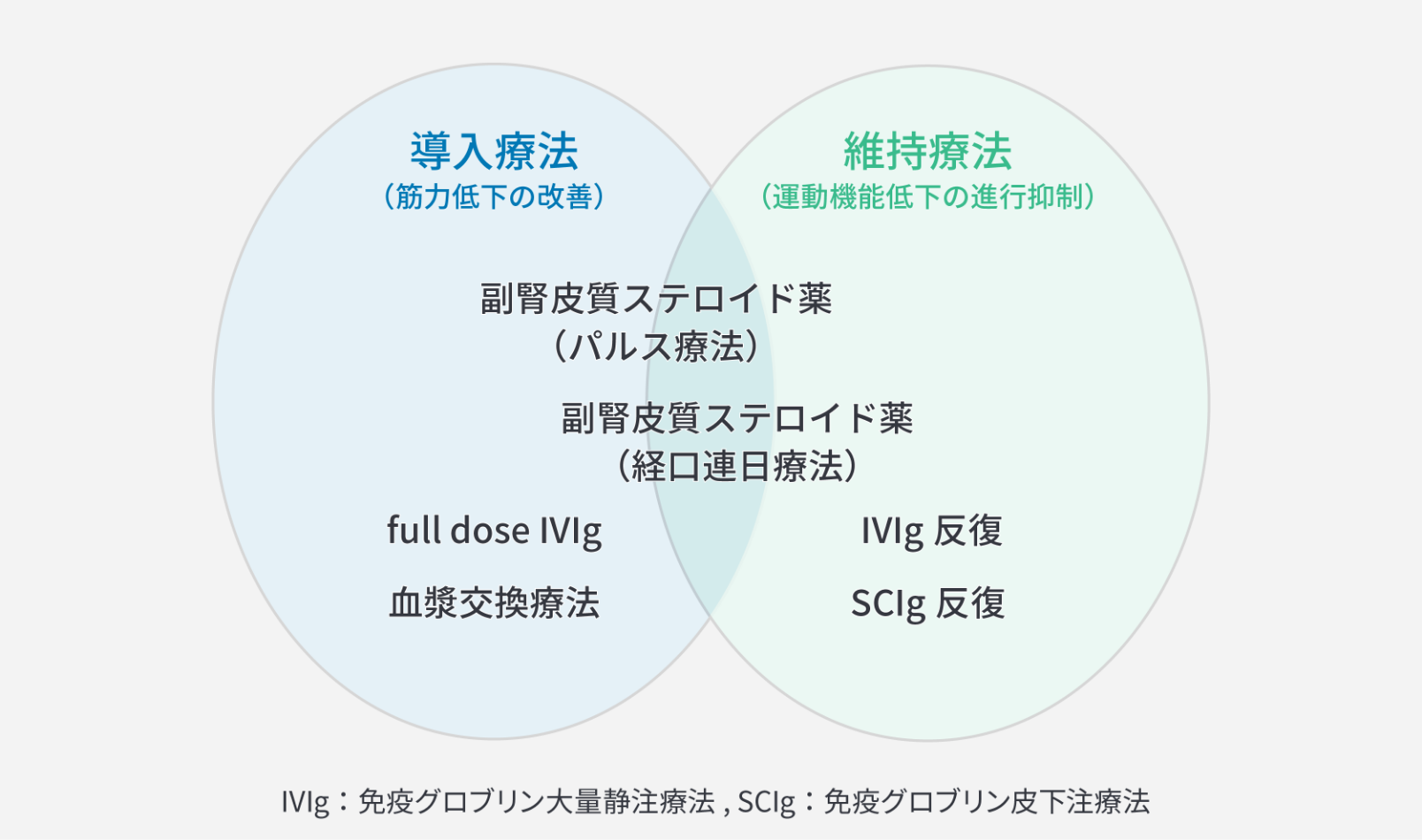
国分則⼈: CIDPの治療,BRAIN and NERVE. 2025,77:43-48.
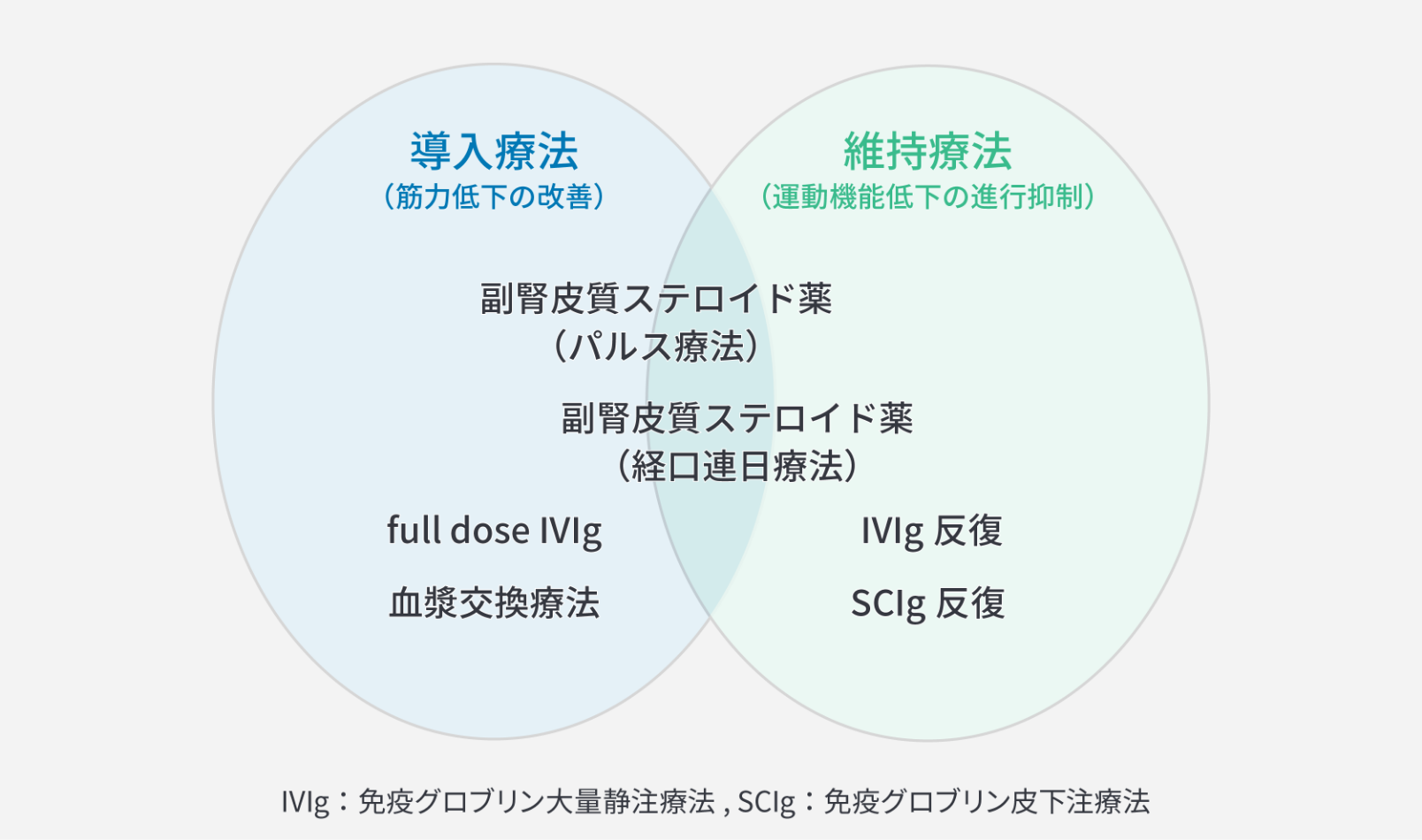
国分則⼈: CIDPの治療,BRAIN and NERVE. 2025,77:43-48.
CIDPの治療効果判定
末梢神経は、軽度の障害であれば再⽣する能⼒を保持しています4)。重要なこととして、現在使⽤されているCIDP治療薬に直接末梢神経の再⽣を促す作⽤機序を持つものはありません。従って、どの治療薬もCIDPの病勢を抑えることが主体となっており、末梢神経の回復は、神経の再⽣能⼒に依存することになります。CIDPでは多くの症例が軸索障害まで⾄っていることが多いため、CIDPの治療効果判定は、神経の再⽣時間を考慮し、少なくとも6ヵ⽉以降に評価を⾏う必要があります4)。判定は「著効」「効果不⼗分(わずかに改善)」「効果不⼗分(変化なし)」「無効(悪化)」の4パターンで⾏い、この結果に基づいて治療継続、治療強度を上げる、他治療法の追加‧変更を決定します4)。「著効」は治療発現時間が早く回復効果が⾼い状態で、現在の治療を継続します4)。「効果不⼗分(わずかに改善)」は治療発現時間が緩やかで回復効果が低い状態であり、治療継続か、治療強度を上げるかを検討します4)。「効果不⼗分(変化なし)」は⼀⾒すると「無効」と判断しがちですが、これまで進⾏してきた症状の進⾏を⽌めている状態と判断できるため、この場合には治療強度を上げる必要性があります4)。治療強度を⾼めても症状の改善がみられない場合は、投与をいったん中断、⼜は投与間隔をあけます。「無効(悪化)」は症状が悪化している状態で、診断の⾒直し、免疫抑制薬の追加‧変更を検討します4)。治療中に6ヵ⽉以上症状の他覚的改善がみられない場合は、⼀旦治療を離脱するか投与間隔を延⻑し、過剰治療(over treatment)を防ぎ、再発の有無を観察‧評価していきます4)。
図3.CIDPの治療スキーム
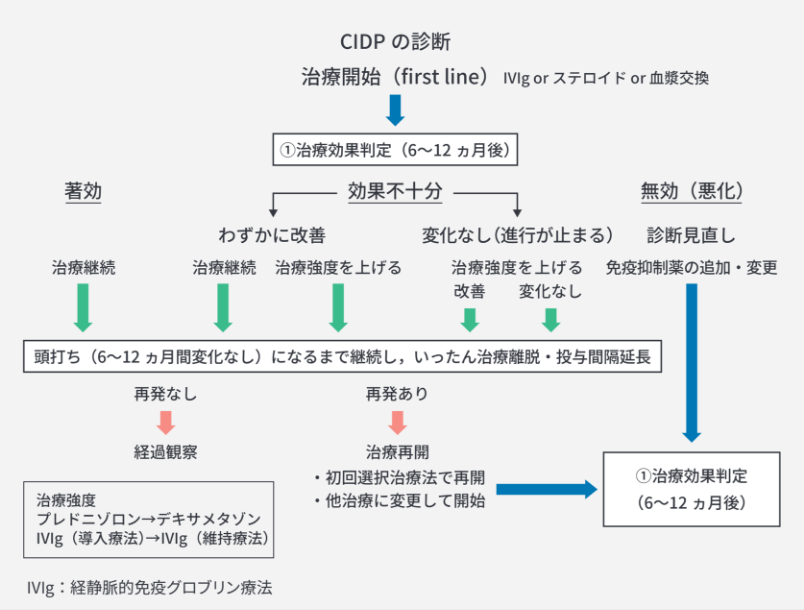
⽵下幸男:CIDPの治療,BRAIN and NERVE. 2025, 77: 49-55.
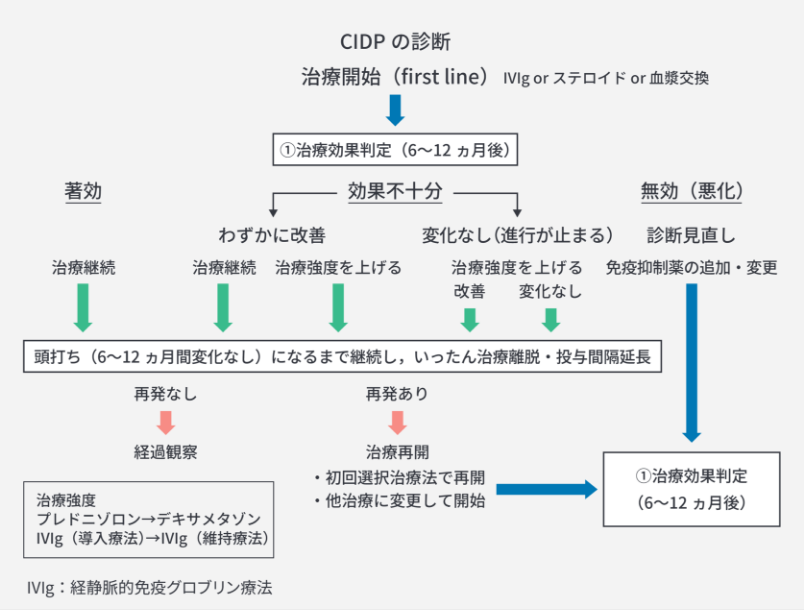
⽵下幸男:CIDPの治療,BRAIN and NERVE. 2025, 77: 49-55.
免疫グロブリン療法
免疫グロブリン療法は、CIDPに対して液性免疫‧細胞性免疫の多⾓的な免疫調整作⽤があると考えられています3)。
免疫グロブリン療法には、免疫グロブリン静注療法(IVIg)と免疫グロブリン⽪下注療法(SCIg)があります。導⼊療法としてIVIgを⾏い、効果が確認された場合は、維持療法としてIVIg⼜はSCIgを⾏うことが推奨されています3)。なお、SCIgには、従来型SCIg(cSCIg: conventional SCIg)と促進型SCIg(fSCIg: facilitated SCIg)の2種類があります。
使⽤⽅法
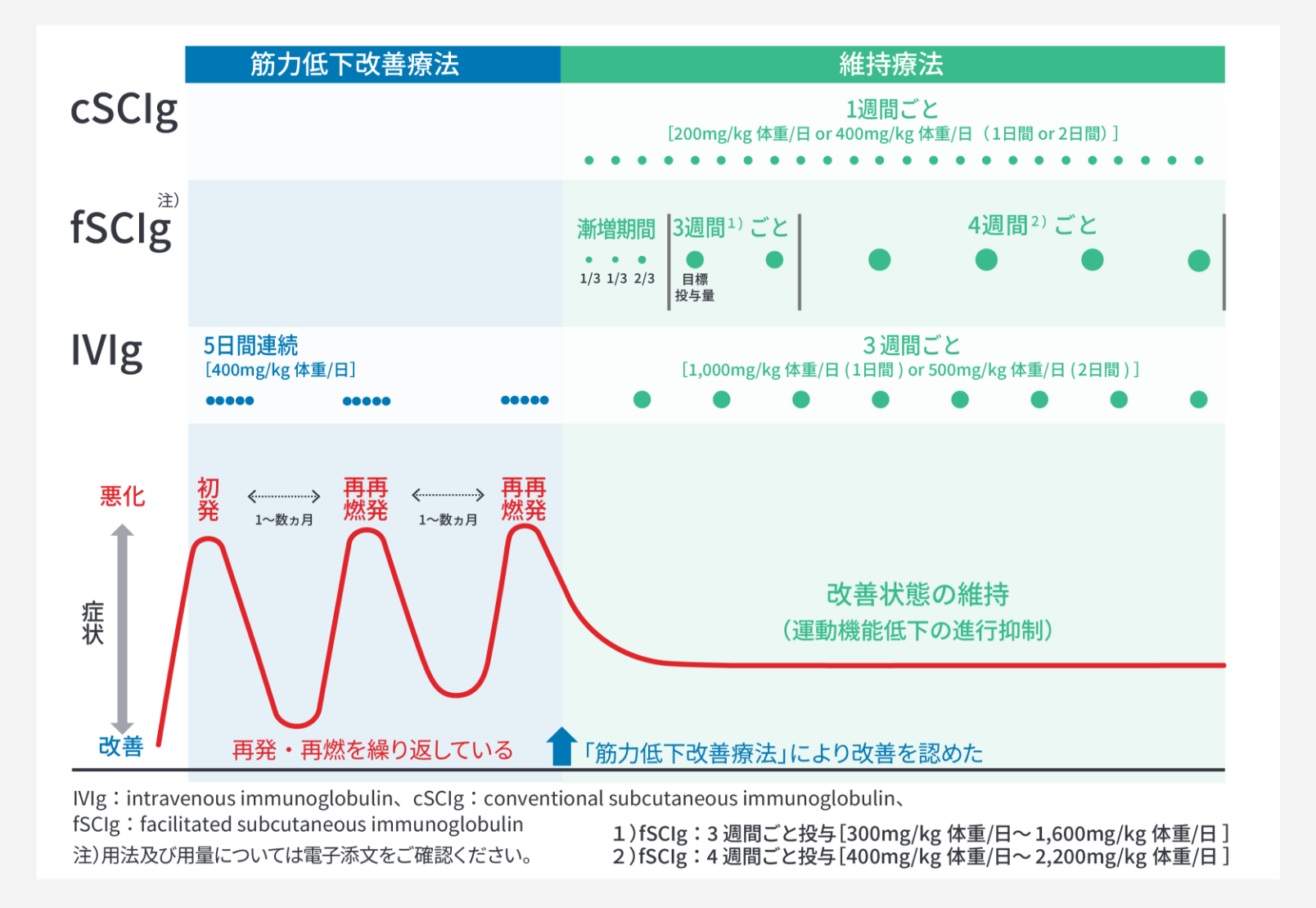
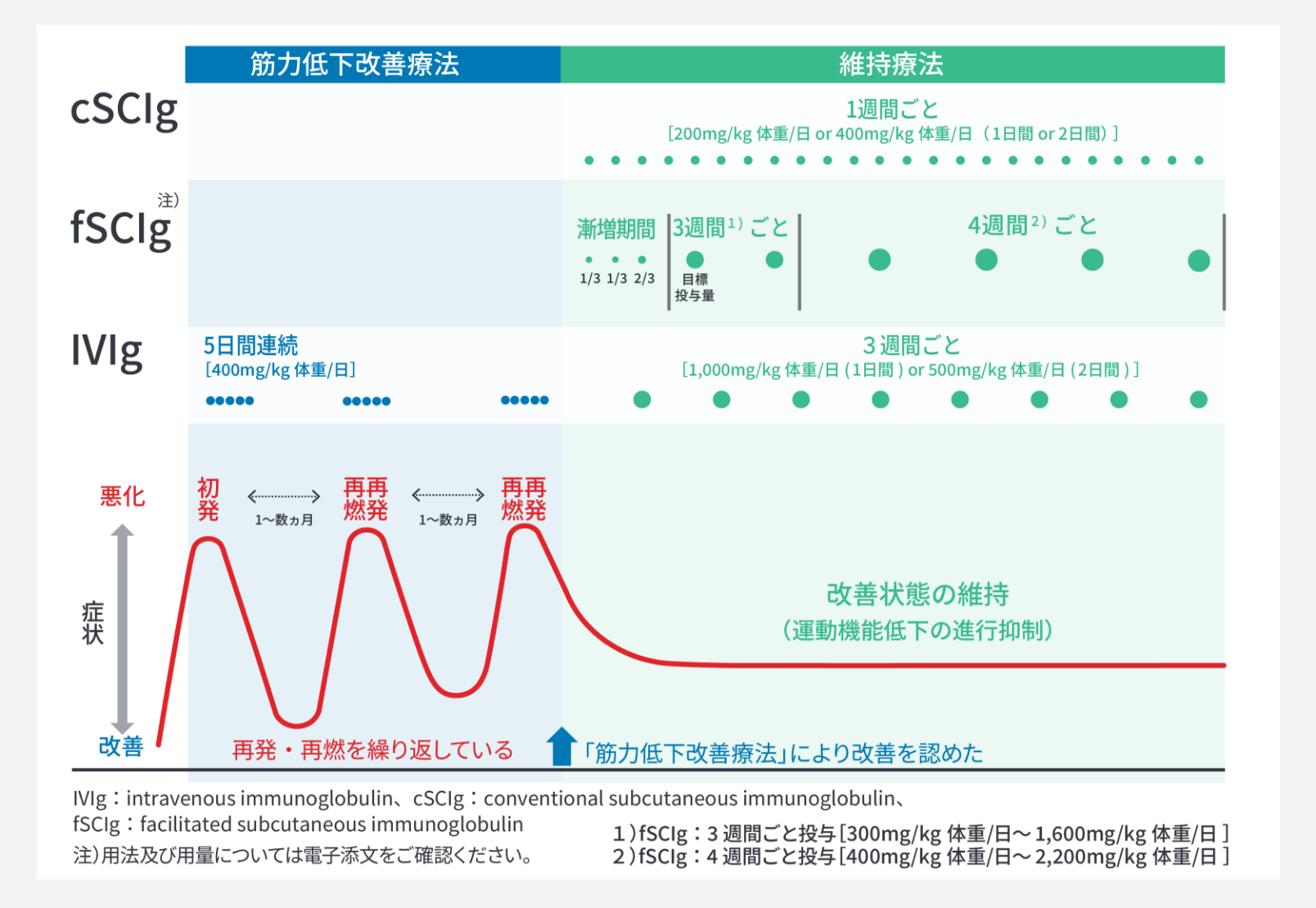
維持療法
⻑期の維持療法は必要ではなく、6ヵ⽉間寛解が持続した場合は、減量‧中⽌を検討します。なお、症状の維持に必要な免疫グロブリン⽤量及び間隔は、個々の患者さんで異なる可能性があります。
なお、免疫グロブリンの維持療法の⽤量は、IVIgの場合は1.0g/kg体重を3週間ごとに投与、cSCIgの場合は0.2g/kg体重を1週間回投与することが適応承認されています。⼀⽅でfSCIgの場合は1.0g/kg体重を3週間に1回投与しますが、患者の状態に合わせて0.3〜1.6g/kg体重を3週間に1回、⼜は0.4〜2.2g/kg体重を4週間に1回の範囲で適宜増減します。
副作⽤
免疫グロブリン療法の重篤な副作⽤として、アレルギー反応及び静脈⾎栓症が報告されています5,6)。これらの重篤な副作⽤は、特に投与開始後1時間以内や投与速度を上げた際に発⽣しやすいことが知られています。また、CIDP以外の疾患を含む調査においても腎機能の悪化が報告されているため、定期的な腎機能の監視が重要です7)。
⾼頻度に認められる副作⽤として、頭痛、嘔気、悪寒、発熱、疲労感、筋⾁痛‧関節痛、⾎圧上昇、軽度の⾎圧低下、発疹、汗疱などがみられます。無菌性髄膜炎は投与開始48〜72時間後に発症することが多く、重篤化する例は少なく、⾃然寛解します3)。
副腎⽪質ステロイド薬
副腎⽪質ステロイド薬の導⼊療法、維持療法として、メチルプレドニゾロン静注パルス、デキサメタゾン経⼝パルスがあります8)。最適な投与レジメンについての⼗分なエビデンスがないため、医師の経験、合併症、患者さんの希望に応じて使い分けています。⻑期にわたる副腎⽪質ステロイド薬治療は、重⼤な副作⽤を引き起こす可能性があるため注意する必要があります3)。
使用方法


副作⽤
副腎⽪質ステロイド薬の⻑期投与による副作⽤として、⾻粗鬆症、⾻壊死、⽩内障、易感染症、創傷治癒遅延、脂肪肝、動脈硬化、⼩児での低⾝⻑などがあります。その他、糖尿病、⾼⾎圧、消化性潰瘍、痤瘡、満⽉様顔貌、⾷欲増進、多⽑、精神病、不眠、発汗、⽉経異常、低カリウム⾎症、ステロイド筋症などが認められます3)。
⽇本⾻代謝学会の「ステロイド性⾻粗鬆症の管理と治療ガイドライン:2014年改訂版」では、腰椎⾻密度が80%未満でステロイド投与量がプレドニゾロン換算で5mg/⽇以上のステロイド薬使⽤時には予防治療を推奨しています11)。
プレドニゾロン20mg/⽇の連⽇投与で感染症リスクが2倍となります。特にニューモシスチス肺炎と結核に注意が必要です。免疫抑制状態の⾮HIV患者では、ST合剤の予防投与でニューモシスチス肺炎の85%を予防できます12)。
⾎漿浄化療法
⾎漿浄化療法は、免疫グロブリン静注療法(IVIg)と副腎⽪質ステロイド薬と同等の有効性が認められている13)ため強く推奨されています。ただし、体外循環を要することから第⼆選択の治療に位置づけられています3)。
⾎漿浄化療法には、単純⾎漿交換、免疫吸着法、⼆重膜濾過法がありますが、CIDPの治療において有効性が実証されているのは単純⾎漿交換のみです3)。
単純⾎漿交換では、分離した⾎漿を除去し、同量の置換液を補充します3)。
使⽤⽅法
連⽇⼜は隔⽇で2週間以上かけて5回実施します13)。⽇本では保険適⽤により、3ヵ⽉間に限り最⼤7回まで算定可能です3)。
副作⽤
⾎漿浄化療法の重篤な副作⽤としては、失神や低⾎圧が報告されています。その他の副作⽤として、ブラッドアクセスのトラブルが報告されています14)。ブラッドアクセスについては、末梢⾎管の使⽤が推奨されています13)。
その他の治療法
ガイドラインにおいては⼀次治療抵抗例には下記の対応を検討することとなっています。
免疫抑制薬
標準的治療(免疫グロブリン静注療法[IVIg]、副腎⽪質ステロイド薬、⾎漿浄化療法)で病勢をコントロールできない場合や、何らかの理由で標準的治療法が使⽤できない場合は、追加治療法⼜は補助的治療法として免疫抑制薬の使⽤が考慮されています3)。
免疫抑制薬としてシクロホスファミドとシクロスポリン※、アザチオプリン※が挙げられていますが、⽇本国内ではシクロホスファミドのみが保険診療として認められています3)。
※国内未承認
分⼦標的治療
分⼦標的治療として、リツキシマブ、胎児型Fc受容体阻害薬があります。リツキシマブは保険適⽤外です3)。胎児型Fc受容体阻害薬は、抗体の分解抑(再利⽤)に関わるFcRnを阻害することにより抗体の分解を促進します。
その結果⾃⼰抗体を減少させ、症状を改善させます15)。また、2024年12⽉に抗FcRn抗体フラグメント‧ヒアルロン酸分解酵素配合製剤がCIDPの適応を取得しており、新たな治療選択肢が登場しました。
リハビリテーション
リハビリテーションにより、運動機能の回復だけでなく、疲労や⼼理的側⾯などを含む総合的な⾝体機能の改善をもたらす可能性があり、有効とされています3)。
他の疾患と同様に、急性期には関節の屈曲拘縮や過伸展を防ぎ、関節可動域を維持するなど、廃⽤症候群の予防が重要です。治療により病勢がコントロールされた後も、臨床病型によって障害部位や症状が異なるため、病型に留意しながら廃⽤と障害筋の過⽤に注意してリハビリテーションを実施します3)。
参考⽂献
1)海⽥賢⼀: CIDPの治療戦略, ⽇本臨牀. 2022, 80(増刊号5): 253-259.
2)国分則⼈: CIDPの治療,BRAIN and ERVE. 2025,77:43-48.
3)⽇本神経学会(監): 慢性炎症性脱髄性多発根ニューロパチー, 多巣性運動ニューロパチー診療ガイドライン 2024, 南江堂.2024: 30-43, 86-88, 128-146.
4)⽵下幸男: CIDPの治療,BRAIN and ERVE. 2025,77:49-55.
5)Stangel M, et al.: J Neurol. 2003;250(7):818-821.
6)Wittstock M, et al.: Eur Neurol. 2003;50(3):172-175.
7)Sekul EA, et al.: Ann Intern Med.1994;121(4):259-262.
8)Van den Bergh PYK, et al.: Eur J Neurol. 2021;28(11):3556-3558.
9)van Schaik IN, et al.: Lancet Neurol. 2010;9(3):245-253.
10)Eftimov F, et al.: Neurology. 2012;78(14):1079-1084.
11)⽇本⾻代謝学会(編): ステロイド性⾻粗鬆症の管理と治療ガイドライン: 2014年改訂版(和⽂概略版), 2014, 1-8.
12)Stern A, et al.: Cochrane Database Syst Rev. 2014;2014(10):CD005590.
13)Van den Bergh PYK, et al.: J Peripher Nerv Syst. 2021;26(3):242-268.
14)Henriksson M, et al.: Transfus Apher Sci. 2016;54(1):2-15.
15)抗FcRn 抗体フラグメント‧ヒアルロン酸分解酵素配合製剤の電⼦添⽂